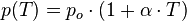La temperatura influenza la pressione di un gas reale (in questo caso l'aria). Quindi da un punto di vista teorico si ha una variazione di pressione al variare della temperatura. Da un punto di vista pratico (ossia legato alla pressione dell'aria nella camera della forcella )si ha una variazione di pressione che non influisce eccessivamente sul funzionamento della forcella stessa, soprattutto per variazioni di temperatura stagionali (nell'ordine di 10°C).
Possiamo (approssimando) considerare l'aria come un gas perfetto.
A questo punto vale la seconda legge di Gay-Lussac (trasformazione isocora o a volume costante)
Indicando con
P0 la pressione di un gas alla temperatura di 0°C e con P
(T
) la pressione ad una temperatura maggiore di 0. Il parametro
α è detto
coefficiente di espansione dei gas e vale per tutti i gas circa 3.663
10-3 °C -1, pari a circa 1/273 °C -1. α rappresenta quindi l'aumento relativo di pressione subito dal gas quando la sua temperatura aumenta di 1°C.
Ad esempio, se la temperatura del gas aumenta da 0 a 30°C, la pressione del gas a 30°C è
P(30) =
P0(1+0.003663*30) =1.10989
P0; la pressione del gas aumenta cioè del 10% circa.
Ciò significa che se la forcella era caricata a 0°C 125psi si trovera a 30°C ad un pressione di 137,5psi